Ανόργανη Χημεία (Θ)
Χριστίνα Φούντζουλα
Σκοπός του μαθήματος είναι να δοθούν στους φοιτητές οι βασικές θεωρητικές και πρακτικές γνώσεις Ανόργανης Χημείας, με σκοπό την κατανόηση και εμπέδωση βασικών χημικών και φυσικοχημικών εννοιών και την απόκτηση του απαραίτητου υποβάθρου για την εμβάθυνση σε εξειδικευμένα γνωστικά αντικείμενα του προγράμματος σπουδών.
Οι εργαστηριακές ασκήσεις συμβάλλουν σημαντικά στην κατανόηση της χρήσης της επιστημονικής μεθοδολογίας και στην απόκτηση πειραματικών και αναλυτικών δεξιοτήτων.
ΛιγότεραΣκοπός του μαθήματος είναι να δοθούν στους φοιτητές οι βασικές θεωρητικές και πρακτικές γνώσεις Ανόργανης Χημείας, με σκοπό την κατανόηση και εμπέδωση βασικών χημικών και φυσικοχημικών εννοιών και την απόκτηση του απαραίτητου υποβάθρου για την εμβάθυνση σε εξειδικευμένα γνωστικά αντικείμενα του προγράμματος σπουδών.
Οι εργαστηριακές ασκήσεις συμβάλλουν σημαντικά στην κατανόηση της χρήσης της επιστημονικής μεθοδολογίας και στην απόκτηση πειραματικών και αναλυτικών δεξιοτήτων.
Σκοπός του μαθήματος είναι να δοθούν στους φοιτητές οι βασικές θεωρητικές και πρακτικές γνώσεις Ανόργανης Χημείας, με σκοπό την κατανόηση και εμπέδωση βασικών χημικών και φυσικοχημικών εννοιών και την απόκτηση του απαραίτητου υποβάθρου για την εμβάθυνση σε εξειδικευμένα γνωστικά αντικείμενα του προγράμματος σπουδών.
Οι εργαστηριακές ασκήσεις συμβάλλουν σημαντικά στην κατανόηση της χρήσης της επιστημονικής μεθοδολογίας και στην απόκτηση πειραματικών και αναλυτικών δεξιοτήτων.

Άτομα, Μόρια και Ιόντα - Εισαγωγή στην κβαντική θεωρία - Το ατομικό πρότυπο του Bohr - Δυϊσμός κύματος /σωματιδίου - Αρχή της αβεβαιότητας - Κβαντικοί αριθμοί και ατομικά τροχιακά - Πολυηλεκτρονικά άτομα - Ηλεκτρονικές διατάξεις και περιοδικό σύστημα.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής βασικές έννοιες της Χημείας όπως η δομή του ατόμου και η λογική δόμησης του περιοδικού συστήματος.
Λέξεις Κλειδιά
Άτομο, υποατομικά σωματίδια, ατομικός και μαζικός αριθμός, ισότοπα, ατομικά πρότυπα, αρχή της αβεβαιότητας του Heisenberg, κβαντικοί αριθμοί, τομείς s, p, d και f.
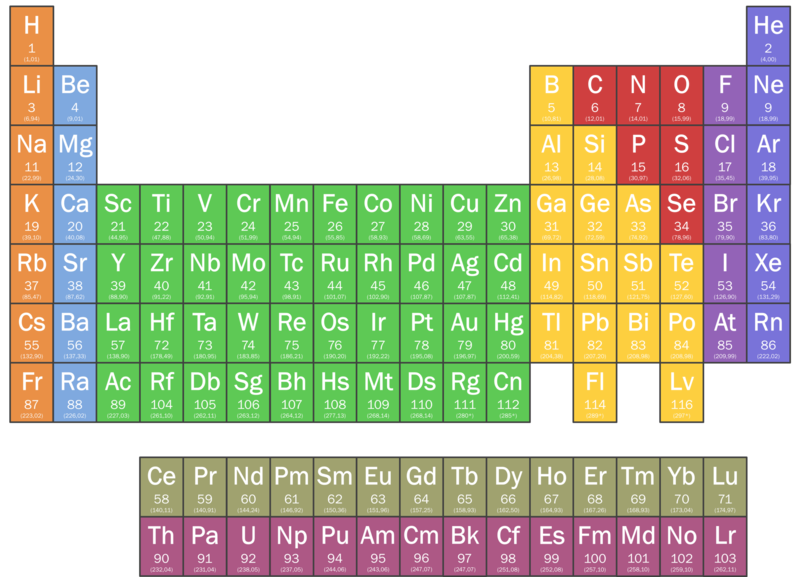
Ο σύγχρονος Περιοδικός Πίνακας - Τα μέταλλα, τα αμέταλλα και τα ιόντα τους - Τα μεγέθη των ατόμων και ιόντων - Ενέργεια ιοντισμού και ηλεκτρονική συγγένεια - Μαγνητικές ιδιότητες - Περιοδικότητα στις ιδιότητες των στοιχείων- Βιολογική σημασία ορισμένων στοιχείων.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής βασικές ιδιότητες των ατόμων και ιόντων όπως το μέγεθος, η ενέργεια ιοντισμού και η ηλεκτρονική συγγένεια καθώς και πως αυτές μεταβάλλονται μέσα στο περιοδικό σύστημα συνδυάζοντας έτσι την περιοδικότητα των ιδιοτήτων με φυσικές και χημικές ιδιότητες των στοιχείων.
Λέξεις Κλειδιά
Αλκάλια, αλκαλικές γαίες, μέταλλα, αμέταλλα, αλογόνα, ευγενή αέρια, κατιόντα, ανιόντα, ατομική ακτίνα, ενέργεια ιοντισμού, ηλεκτρονική συγγένεια.
Οξέα, βάσεις, άλατα, διάσταση ηλεκτρολυτών, ιοντισμός ηλεκτρολυτών, Οξέα – Βάσεις κατά Arrhenius, Οξέα – Βάσεις κατά Brönsted-Lowry και Lewis, Ταξινόμηση των οξέων.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τα κοινά χαρακτηριστικά οξέων και βάσεων και να συσχετισθούν οι όξινες και βασικές ιδιότητες μιας ουσίας με τη δομή της.
Λέξεις Κλειδιά
Θεωρία Arrhenius, θεωρία Brönsted-Lowry, θεωρία Lewis, Οξέα και βάσεις κατά Arrhenius, Brönsted-Lowry και Lewis.
Ισορροπία σε διάλυμα, Συγκέντρωση διαλυμάτων, Μετατροπή μεταξύ εκφράσεων συγκέντρωσης, Πορεία της διάλυσης, Διάλυση αερίων σε υγρά, Εξάρτηση της διαλυτότητας από τη θερμοκρασία, Κολλοειδή Διαλύματα.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τις έννοιες του διαλύματος και της περιεκτικότητας αυτού σε διαλυμένη(ε)ς ουσία(ε)ς και τους τρόπους έκφρασης της συγκέντρωσης διαλύματος.
Λέξεις Κλειδιά
Διαλυτότητα ουσιών, συγκέντρωση διαλύματος, γραμμομοριακότητα κατ’όγκο (molarity), κανονικότητα (normality), κατά βάρος περιεκτικότητα, κατ’όγκο περιεκτικότητα.
Η ισορροπία στις χημικές αντιδράσεις- Ομογενείς και ετερογενείς αντιδράσεις- Νόμος Δράσης των Μαζών- Κατεύθυνση και σταθερά χημικής ισορροπίας- Παράγοντες που επηρεάζουν την κατεύθυνση της χημικής ισορροπίας.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τις αρχές της χημικής ισορροπίας και τους παράγοντες που επηρεάζουν τη θέση της ισορροπίας.
Λέξεις Κλειδιά
Ομογενείς και ετερογενείς αντιδράσεις, αρχή Le Chatelier.
Ρυθμιστική ικανότητα, αραίωση, ενδοκυττάρια και εξωκυττάρια ρυθμιστικά συστήματα, όξινα και δισόξινα φωσφορικά ιόντα.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής την έννοια του ιοντισμού ασθενών οξέων και βάσεων καθώς και τους παράγοντες που τον επηρεάζουν.
Λέξεις Κλειδιά
Ιοντισμός, pH ρυθμιστικού διαλύματος.
Ιοντισμός ασθενών οξέων και βάσεων, βαθμός ιοντισμού, σταθερά ιοντισμού ασθενούς μονοπρωτικού οξέος, σχέση μεταξύ των σταθερών ιοντισμού ασθενούς μονοπρωτικού οξέος και ασθενούς μονοπρωτικής βάσης.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τον ιοντισμό ασθενούς μονοπρωτικού οξέος αλλά και τη σχέση μεταξύ των σταθερών ιοντισμού ασθενούς μονοπρωτικού οξέος και ασθενούς μονοπρωτικής βάσης.
Λέξεις Κλειδιά
Σταθερά ιοντισμού ασθενούς μονοπρωτικού οξέος.
Ιοντισμός μονοπρωτικών οξέων, Ιοντισμός πολυπρωτικών οξέων, Βαθμός ιοντισμού, pH και pOH.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τη συμπεριφορά ισχυρών οξέων και βάσεων, τις έννοιες του pH και pOH και την εξάρτησή τους από τη θερμοκρασία.
Λέξεις Κλειδιά
pH και pOH.
Οξείδωση/ Αναγωγή- Οξειδωτικά και αναγωγικά σώματα- Αριθμός οξείδωσης- Ισοστάθμιση ημιαντιδράσεων οξείδωσης, αναγωγής και αντιδράσεων οξειδοαναγωγής- Σειρά αναγωγικής/οξειδωτικής ισχύος.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τις αρχές του οξειδοαναγωγικού φαινομένου.
Λέξεις Κλειδιά
Οξείδωση, Αναγωγή, Οξειδωτικά και αναγωγικά σώματα, Αριθμός οξείδωσης ημιαντιδράσεις οξείδωσης και αναγωγής, αναγωγική/οξειδωτική ισχύς σωμάτων.
Ιδανικά και μη ιδανικά διαλύματα - Νόμος του Raoult - Ελάττωση της τάσης ατμών του διαλύτη - Ανύψωση του σημείου ζέσεως - Ταπείνωση του σημείου πήξεως - Ώσμωση, ωσμωτική πίεση και διύλιση - Λειτουργία μονάδας τεχνητού νεφρού.
Στόχοι Ενότητας
Να κατανοήσει ο φοιτητής τις προσθετικές ιδιότητες των διαλυμάτων.
Λέξεις Κλειδιά
Νόμος του Raoult, ζεσεοσκοπία, κρυοσκοπία, ώσμωση, μονάδα τεχνητού νεφρού.
Ανοικτό Ακαδ. Μάθημα

Αρ. Επισκέψεων : 3719
Αρ. Προβολών : 22971
Ημερολόγιο
Ανακοινώσεις
- - Δεν υπάρχουν ανακοινώσεις -